Category: Nghiên cứu Tế bào gốc
-
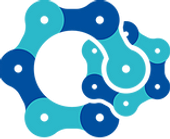
Cấy ghép tế bào gốc thần kinh cho thấy triển vọng trong điều trị chấn thương tuỷ sống mãn tính
Một thử nghiệm lâm sàng giai đoạn I do các nhà nghiên cứu tại Trường Y, Đại học California San Diego dẫn đầu đã chứng minh tính an toàn và khả thi lâu dài của việc cấy ghép tế bào gốc thần kinh để điều trị chấn thương tuỷ sống mạn tính. Những chấn thương…
-
Những Khám Phá Mới Trong Nghiên Cứu Khoa Học: Mở Ra Chân Trời Mới Với Công Nghệ Bảo Quản Đông Lạnh và Tăng Sinh Tế Bào NK-92
Trong lĩnh vực y học hiện đại, những bước tiến quan trọng đã được ghi nhận trong nghiên cứu về dòng tế bào NK-92 – một loại tế bào tiêu diệt tự nhiên có tiềm năng lớn trong điều trị ung thư. Nghiên cứu mới nhất đã chứng minh thành công trong việc tăng sinh…
-
Tiến Bộ Mới Trong Nghiên Cứu Khoa Học: Vai Trò Của IL-1α Trong Xơ Hóa Phổi Và Gan
Một nghiên cứu đột phá gần đây đã làm sáng tỏ vai trò đặc biệt của cytokine interleukin 1 alpha (IL-1α) trong quá trình xơ hóa phổi và gan. Nghiên cứu này, được công bố trên tạp chí International Immunopharmacology với tiêu đề “Processing of angiocrine alarmin IL-1α in endothelial cells promotes lung and liver…
-
Liệu pháp tế bào gốc trong điều trị bệnh ly thượng bì bọng nước: Kết quả khác nhau ở từng bệnh nhân
Liệu pháp tế bào gốc trong điều trị bệnh ly thượng bì bọng nước đang cho thấy những kết quả đầy hứa hẹn, tuy nhiên hiệu quả điều trị có sự khác biệt giữa các bệnh nhân. Bệnh ly thượng bì bọng nước (Epidermolysis Bullosa – EB) là một nhóm bệnh hiếm gặp gây ra…
-
Liệu pháp tế bào gốc mở ra hy vọng điều trị bệnh Hirschsprung
Bệnh Hirschsprung là một dị tật bẩm sinh hiếm gặp, ảnh hưởng đến khoảng 1 trên 5000 trẻ sơ sinh, do sự thiếu hụt tế bào thần kinh trong ruột dưới, thường là ở đại tràng. Điều này khiến ruột mất khả năng co bóp bình thường, gây ra tắc nghẽn chức năng và dẫn…
-
Xác định “mảnh ghép còn thiếu” giúp tế bào gốc máu duy trì khả năng tự đổi mới
Tế bào gốc máu là nền tảng cho các liệu pháp cấy ghép, giúp điều trị nhiều bệnh lý nghiêm trọng như ung thư máu, rối loạn máu và rối loạn miễn dịch. Chúng có khả năng tự làm mới và biệt hóa thành các loại tế bào máu khác nhau. Tuy nhiên, khi được…
-
Mô hình chuyển đổi tế bào gốc thành tế bào não: Đột phá trong chẩn đoán và điều trị bệnh Parkinson
Bệnh Parkinson là một rối loạn thoái hóa thần kinh gây ảnh hưởng đến vận động, với các triệu chứng như run rẩy, cứng cơ, suy giảm khả năng nói và các biến chứng thần kinh khác. Một trong những nguyên nhân chính gây ra bệnh là sự tích tụ và gấp cuộn sai của…
-
Trường hợp thứ 7 khỏi bệnh HIV sau khi cấy ghép tế bào gốc để điều trị bệnh bạch cầu
Một người đàn ông ở Đức không còn phát hiện thấy HIV trong cơ thể sau khi được điều trị vào năm 2015. Đây là bệnh nhân thứ 7 được chữa khỏi HIV sau khi điều trị bệnh bạch cầu. Trước đó, chỉ có 6 trường hợp tương tự được ghi nhận trong 40 năm…
-
Phụ Nữ Ghép Tế Bào Gốc Tạo Máu Đồng Loài Có Thể Mang Thai và Sinh Con Khỏe Mạnh
Việc mang thai sau khi cấy ghép tế bào gốc tạo máu đồng loài để điều trị ung thư từng được cho là gần như không thể. Tuy nhiên, nghiên cứu mới công bố trên tạp chí Blood cho thấy rằng bệnh nhân nữ vẫn có thể mang thai và sinh con khỏe mạnh sau…
-
Đột Biến Sửa Chữa DNA Hoạt Động Như Một Công Tắc Cho Bệnh Ung Thư Ruột
Các tế bào ung thư ruột có khả năng điều chỉnh sự phát triển của chúng bằng cách sử dụng một cơ chế “bật/tắt” di truyền để tối đa hóa cơ hội sống sót. Hiện tượng này lần đầu tiên được quan sát bởi các nhà nghiên cứu tại UCL và Trung tâm Y tế…