
Sự phát triển vũ bão của các liệu pháp trị liệu tiên tiến (ATMP) đã đặt các cơ quan quản lý dược phẩm hàng đầu thế giới vào một tình thế đòi hỏi sự thay đổi tư duy quản lý. Vào ngày 11 tháng 1 năm 2026, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã công bố một bản cập nhật quan trọng về tính linh hoạt trong các yêu cầu Hóa học, Sản xuất và Kiểm soát (CMC) đối với các sản phẩm ATMP.
Ủy viên FDA, ông Marty Makary, cho biết việc nới lỏng các yêu cầu sản xuất đối với một số liệu pháp tế bào và gen là “những cải cách thông thường” nhằm thúc đẩy sự đổi mới.

FDA: Tư duy quản lý dựa trên đặc tính tế bào
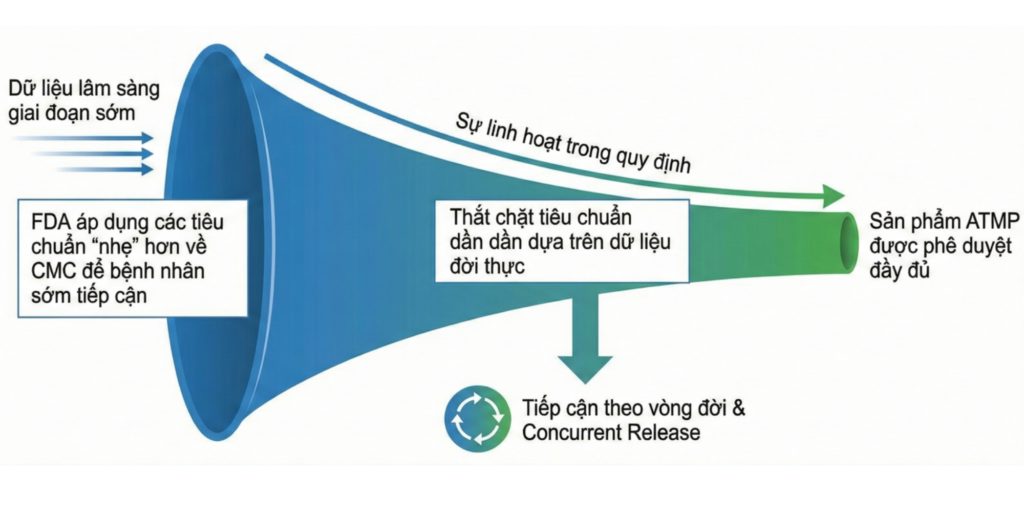
Hình: Mô hình phê duyệt thích ứng của FDA cho ATMP. Một biểu đồ hình phễu thể hiện sự linh hoạt. Ở đầu vào là dữ liệu lâm sàng giai đoạn sớm, FDA áp dụng các tiêu chuẩn “nhẹ” hơn về CMC để bệnh nhân sớm tiếp cận, sau đó thắt chặt tiêu chuẩn dần dần dựa trên dữ liệu đời thực.
Trước đây, các quy định CMC thường được áp dụng một cách cứng nhắc tương tự như đối với các loại thuốc hóa dược truyền thống, điều này gây khó khăn lớn cho các liệu pháp tế bào vốn mang tính cá thể hóa cao và có quy trình sản xuất phức tạp.
FDA hiện đã thừa nhận rằng đối với những bệnh lý hiếm hoặc đe dọa tính mạng mà ATMP nhắm tới, việc yêu cầu đầy đủ các lô sản xuất kiểm chuẩn quy mô lớn là không khả thi.
Các điểm mới mang tính đột phá trong hướng dẫn của FDA bao gồm

Trung Quốc và Quy định Y sinh mới 2026
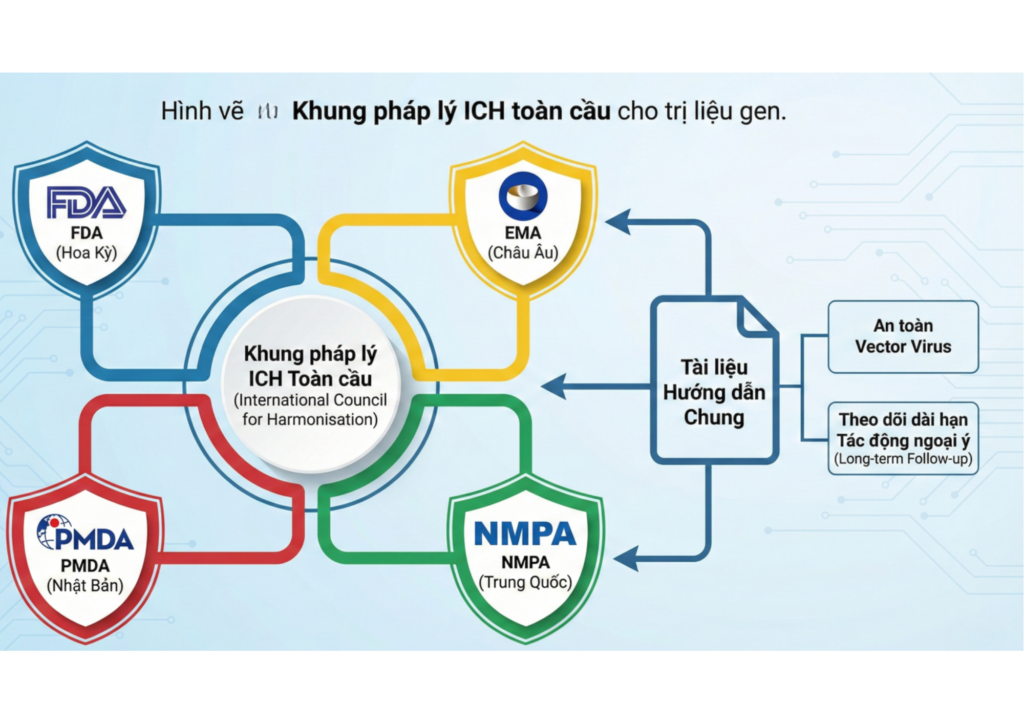
Hình: Khung pháp lý ICH toàn cầu cho trị liệu gen. Một mạng lưới kết nối FDA, EMA, PMDA và NMPA, với các tài liệu hướng dẫn chung về an toàn vector virus và theo dõi dài hạn các tác động ngoại ý
Song song với Hoa Kỳ, Trung Quốc đã ban hành “Quy định Hành chính về Nghiên cứu Lâm sàng và Chuyển đổi Lâm sàng các Công nghệ Y sinh mới”, chính thức có hiệu lực từ ngày 1 tháng 5 năm 2026. Quy định này lần đầu tiên thiết lập một khung quản lý thống nhất cho các công nghệ tiên tiến như tế bào gốc, chỉnh sửa gen và CAR-T. Điểm đặc biệt là Trung Quốc yêu cầu các nghiên cứu này phải được thực hiện tại các bệnh viện hạng 3 có hệ thống hội đồng đạo đức và quản lý rủi ro độc lập, đồng thời thắt chặt việc tham gia của các tổ chức có vốn đầu tư nước ngoài thông qua các thực thể pháp lý tại địa phương.
Sự hài hòa hóa toàn cầu cũng đang được thúc đẩy thông qua Hội nghị quốc tế về hài hòa hóa các thủ tục đăng ký dược phẩm sử dụng cho con người (ICH). Các tài liệu được thông qua vào tháng 11 năm 2025 nhấn mạnh nhu cầu về các hướng dẫn chuyên biệt cho việc theo dõi dài hạn (LTFU) lên tới 15 năm cho bệnh nhân trị liệu gen. Những thay đổi này phản ánh một thực tế: để ATMP trở thành hiện thực, các quy định không thể là rào cản mà phải là “bệ đỡ” cho sự đổi mới an toàn.