Hội nghị thường niên lần thứ 67 của Hiệp hội Huyết học Hoa Kỳ (ASH 2025), diễn ra từ ngày 6 đến 9 tháng 12 năm 2025 tại Orlando, Florida, đã chứng kiến một sự thay đổi cơ bản trong triết lý điều trị ung thư máu. Tâm điểm của hội nghị không còn chỉ là các kết quả lâm sàng dài hạn của các loại tế bào CAR-T truyền thống mà là sự xuất hiện đầy ấn tượng của công nghệ “In-vivo CAR-T” — một phương thức tiếp cận cho phép kỹ nghệ hóa trực tiếp các tế bào miễn dịch ngay bên trong cơ thể người bệnh thông qua các vector di truyền thông minh.
Thách thức của quy trình Ex-vivo CAR-T hiện tại
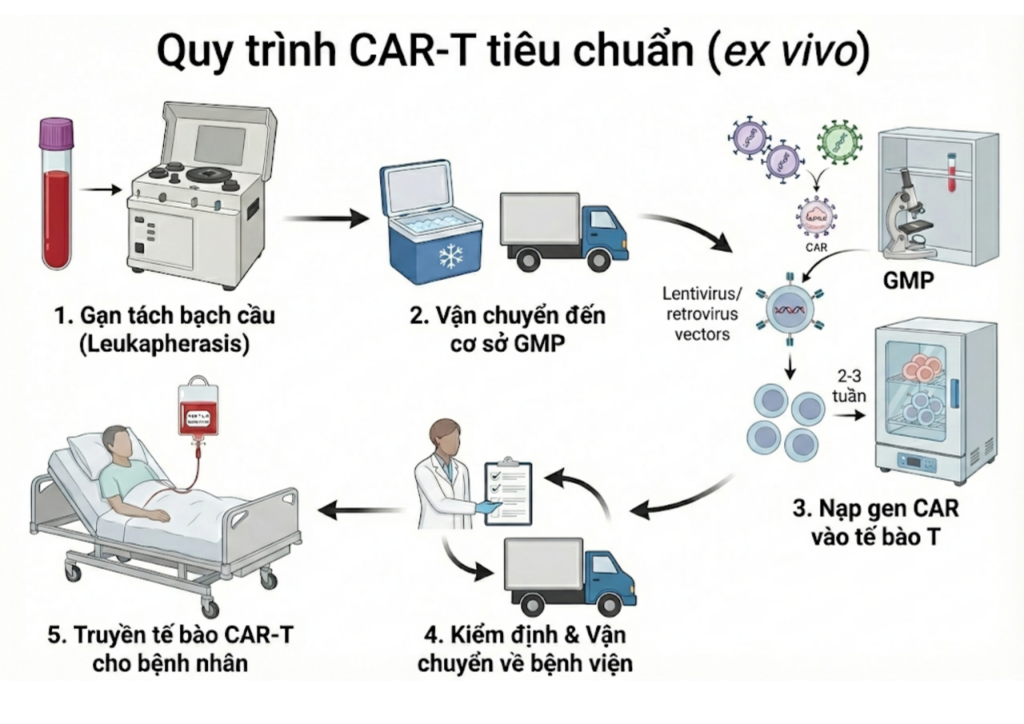
Để hiểu được tầm quan trọng của đột phá này, cần nhìn vào quy trình CAR-T tiêu chuẩn (ex vivo) hiện nay. Bệnh nhân phải trải qua quá trình gạn tách bạch cầu (leukapherasis), sau đó tế bào T được vận chuyển đến một cơ sở sản xuất đạt chuẩn GMP cực kỳ đắt đỏ. Tại đây, lentivirus hoặc retrovirus được sử dụng để nạp gen CAR vào tế bào T, tế bào sau đó được nuôi cấy tăng sinh trong 2-3 tuần trước khi được kiểm định và gửi ngược lại bệnh viện để truyền cho bệnh nhân. Quy trình này không chỉ tốn kém (thường trên 400.000 USD/liều) mà còn tiềm ẩn nguy cơ bệnh tiến triển trong thời gian chờ đợi.
Cơ chế đột phá của VV169: Vector di truyền thông minh
Tại hội nghị ASH 2025, công ty sinh học Vyriad đã thu hút mọi sự chú ý khi công bố dữ liệu tiền lâm sàng của VV169, một ứng viên CAR-T in vivo nhắm mục tiêu BCMA để điều trị đa u tủy xương. VV169 sử dụng một công nghệ vector lentivirus được tinh chỉnh di truyền (LV-169), hoạt động như một “xe tải vận chuyển” di truyền có khả năng nhận diện mục tiêu cực kỳ chính xác.
Cơ chế nhắm mục tiêu của VV169 dựa trên kỹ thuật hiển thị kháng thể đồng hóa trị trực tiếp trên vỏ virus. Các kỹ sư sinh học đã gắn các phân tử nhắm mục tiêu thụ thể CD3 (một dấu ấn đặc trưng của tế bào T) lên bề mặt virus, đồng thời làm virus “mù” hoàn toàn trước các thụ thể LDL thông thường trong cơ thể để tránh sự xâm nhập ngoại ý vào gan hoặc các cơ quan khác. Sau khi tiêm tĩnh mạch, hạt virus này sẽ tự tìm đến và chỉ xâm nhập vào tế bào T của bệnh nhân ngay trong dòng máu hoặc các cơ quan lympho, truyền đoạn mã di truyền CAR và biến chính cơ thể bệnh nhân thành một “nhà máy sản xuất thuốc sống” chỉ trong vài ngày.
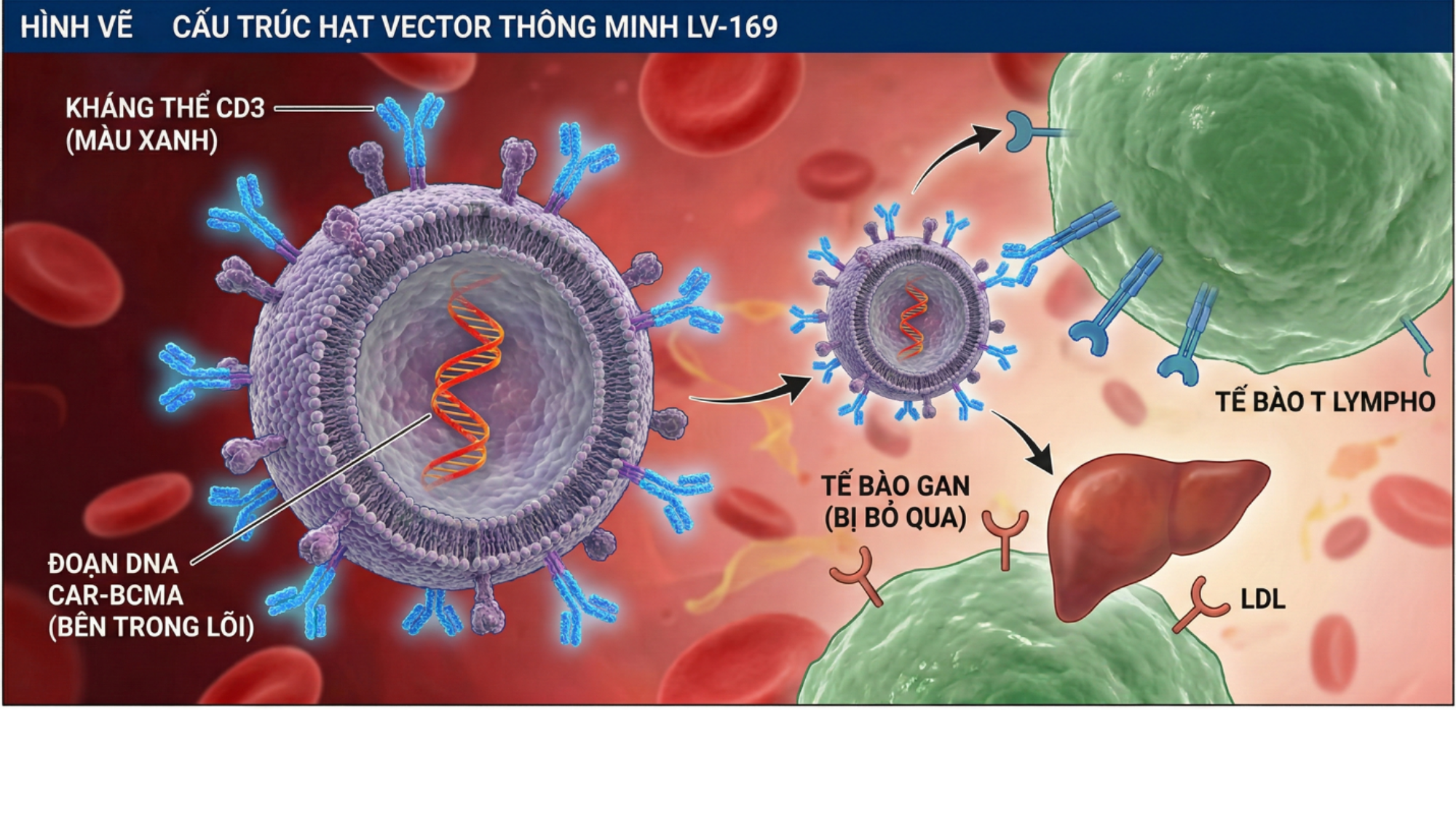
Hình: Cấu trúc hạt vector thông minh LV-169. Một hình vẽ 3D hạt virus. Trên vỏ protein gai là các “ổ khóa” kháng thể CD3 màu xanh. Bên trong lõi chứa đoạn DNA CAR-BCMA. Hình vẽ thể hiện hạt virus đang bỏ qua tế bào gan để bám chặt vào tế bào T lympho.
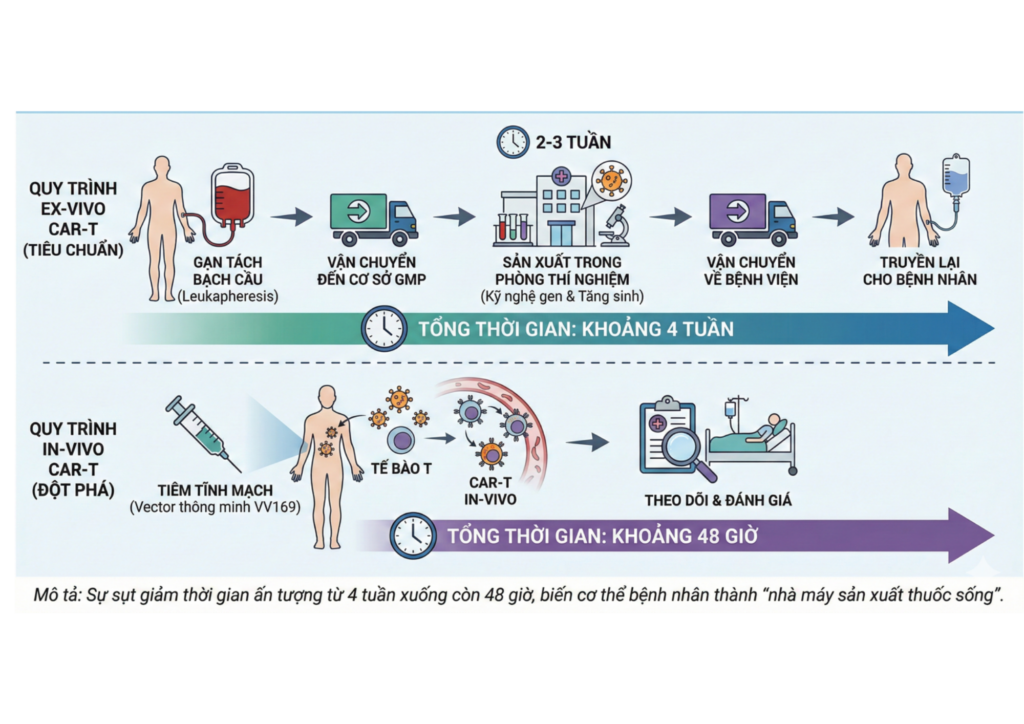
Hình: Quy trình biến cơ thể thành nhà máy CAR-T. Một sơ đồ dòng thời gian so sánh giữa Ex-vivo (trên) và In-vivo (dưới). Quy trình In-vivo chỉ bao gồm 2 bước: Tiêm tĩnh mạch và Theo dõi, nhấn mạnh sự sụt giảm thời gian từ 4 tuần xuống còn 48 giờ.
Kết quả lâm sàng tiền đề và ý nghĩa xã hội
Dữ liệu được trình bày cho thấy 100% chuột mô hình bị đa u tủy xương lan tỏa đã được làm sạch khối u hoàn toàn trong vòng 28 ngày chỉ với một liều duy nhất, kể cả ở mức liều thấp nhất. Phân tích cytokine xác nhận sự vắng mặt của các cơn bão cytokine (CRS) nghiêm trọng, do các tế bào CAR-T được sinh ra một cách dần dần và có kiểm soát hơn so với việc truyền một lượng lớn tế bào đã được kích hoạt từ bên ngoài.
Sự tiến bộ này mang lại hy vọng “dân chủ hóa” việc tiếp cận các phương pháp điều trị ung thư tiên tiến. Thay vì phải đến các trung tâm y tế chuyên sâu tại các thành phố lớn, bệnh nhân có thể nhận liệu pháp in vivo CAR-T dưới dạng một mũi tiêm ngoại trú tại các phòng khám địa phương. Điều này đặc biệt có ý nghĩa đối với các quốc gia đang phát triển, nơi hạ tầng phòng sạch GMP cho tế bào còn hạn chế.
Bên cạnh đó, hội nghị ASH 2025 cũng ghi nhận sức mạnh của các liệu pháp kết hợp. Nghiên cứu MajesTEC-3 cho thấy việc kết hợp teclistamab (kháng thể đặc hiệu đồng thời với BCMA và CD3) với daratumumab mang lại tỷ lệ đáp ứng bền vững lên tới 85% sau 3 năm ở bệnh nhân đa u tủy xương tái phát sớm. Những dữ liệu này đang định hình lại toàn bộ phác đồ điều trị ung thư huyết học cho năm 2026 và xa hơn.