
Vào cuối tháng 10 năm 2025, tại Hội nghị Quốc tế về Bệnh xương thủy tinh (Osteogenesis Imperfecta – OI) diễn ra ở Hồng Kông, cộng đồng y khoa toàn cầu đã đón nhận những kết quả lâm sàng dài hạn tích cực từ thử nghiệm BOOSTB4. Đây là thử nghiệm đầu tiên trên thế giới đánh giá sự kết hợp giữa liệu pháp tế bào gốc trước khi sinh và sau khi sinh để điều trị một trong những căn bệnh di truyền khó khăn nhất đối với trẻ em.
Bệnh xương thủy tinh: Khi cơ thể thiếu hụt “giàn giáo” collagen
Bệnh xương thủy tinh do các đột biến gen (chủ yếu là Col1A1 hoặc Col1A2) gây ra sự thiếu hụt hoặc bất thường về collagen type I — thành phần cấu tạo nên 90% cấu trúc hữu cơ của xương. Hậu quả là xương trở nên cực kỳ giòn, dễ gãy hàng trăm lần ngay cả khi trẻ thực hiện những cử động nhẹ nhất hoặc thậm chí gãy ngay trong tử cung. Hiện tại, chưa có phương pháp điều trị nào có thể chữa khỏi căn nguyên của bệnh, các biện pháp hiện nay chỉ tập trung vào việc giảm thiểu triệu chứng và hỗ trợ vận động.
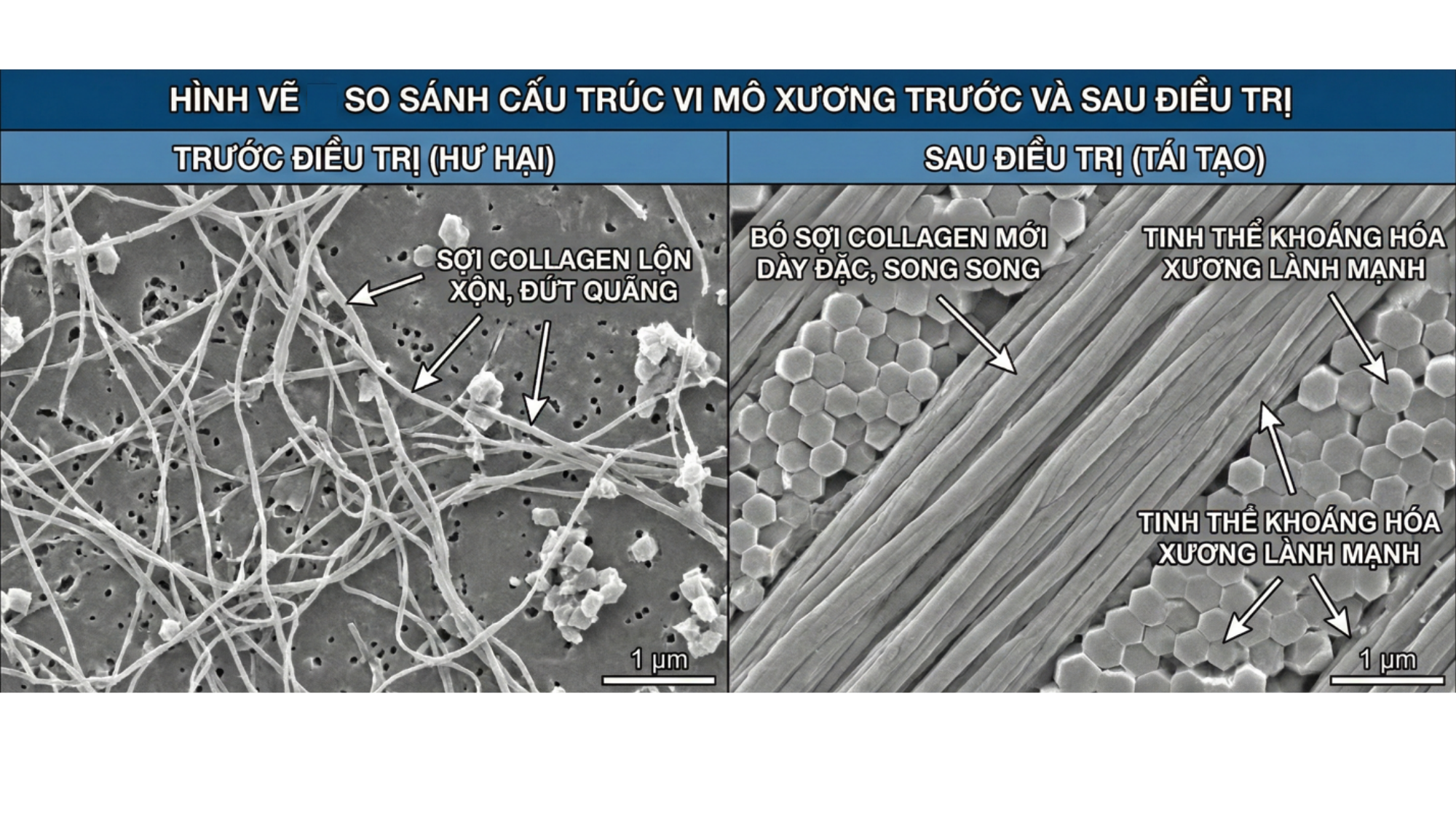
Hình : So sánh cấu trúc vi mô xương trước và sau điều trị. Hình ảnh hiển thị dưới kính hiển vi điện tử. Bên trái (trước điều trị) là các sợi collagen lộn xộn và đứt quãng. Bên phải (sau điều trị) là sự xuất hiện của các bó sợi collagen mới dày đặc, song song, bao quanh bởi các tinh thể khoáng hóa xương khoẻ mạnh.
- Trước điều trị (Hư hại): Sợi collagen lộn xộn, đứt quãng.
- Sau điều trị (Tái tạo): Bó sợi collagen mới dày đặc, song song; tinh thể khoáng hóa xương lành mạnh.
Cơ chế củng cố khung xương của BOOSTB4
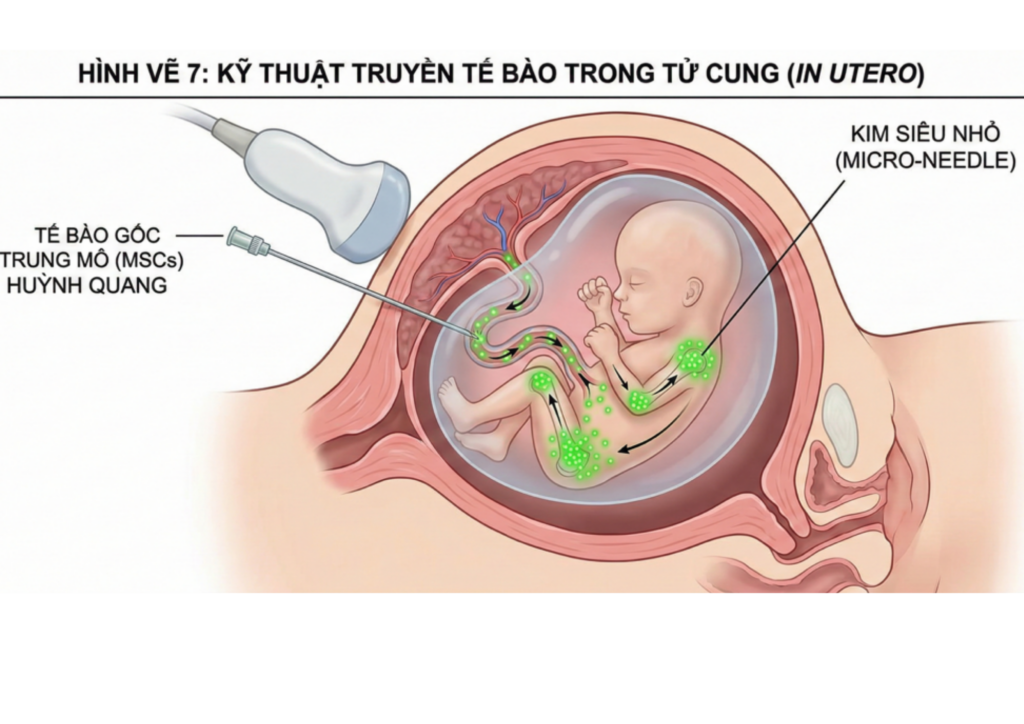
Thử nghiệm BOOSTB4 (Boost Brittle Bones Before Birth) sử dụng tế bào gốc trung mô (MSCs) có nguồn gốc từ gan thai nhi người hiến tặng, vốn là những tế bào có khả năng hình thành xương và sản xuất collagen cực cao. Quy trình can thiệp bao gồm:
- Giai đoạn trước sinh: Truyền MSCs trực tiếp vào tĩnh mạch rốn của thai nhi trong tử cung mẹ dưới sự hướng dẫn của siêu âm vào khoảng tuần thứ 16-35 của thai kỳ.
- Giai đoạn sau sinh: Tiếp tục truyền ba liều bổ sung sau khi trẻ chào đời để duy trì hiệu quả tái tạo.
Các tế bào gốc này có khả năng đặc biệt gọi là “homing” (hướng đích): chúng di chuyển theo dòng máu đến các hốc xương đang phát triển nhanh, biệt hóa thành các nguyên bào xương khỏe mạnh và bắt đầu sản xuất collagen bình thường. Quá trình này tạo ra một “khung xương lai” chắc khỏe hơn, giúp gia cố mật độ xương và giảm đáng kể tính giòn của xương từ bên trong.
Kết quả lâm sàng: Sự thay đổi cuộc đời bền vững
Kết quả theo dõi hai năm cho thấy một bước tiến chưa từng có: liệu pháp đã giúp giảm tới 78% tỷ lệ gãy xương so với giai đoạn trước điều trị. Đặc biệt kinh ngạc là hơn 50% trẻ em tham gia nghiên cứu hoàn toàn không bị gãy xương trong suốt năm thứ hai sau khi kết thúc liệu pháp. Những con số này mang lại một ý nghĩa thay đổi cuộc đời đối với các gia đình bệnh nhân.
Tiến sĩ Cecilia Götherström từ Viện Karolinska, người điều phối nghiên cứu, nhấn mạnh rằng sự thành công của BOOSTB4 là minh chứng cho sức mạnh của sự hợp tác đa ngành và sản xuất tế bào đạt chuẩn GMP. Việc can thiệp sớm ngay từ giai đoạn bào thai giúp tận dụng khả năng tích hợp tế bào gốc vào hệ xương đang hình thành nhanh chóng, mở ra cơ hội cho trẻ em mắc bệnh hiếm được phát triển thể chất một cách bình thường hơn.