
Giải mã rào cản sản xuất tế bào T hỗ trợ để hiện thực hóa kỷ nguyên “Thuốc sống” có sẵn

Tiến sĩ Ross Jones của Đại học British Columbia (UBC) đang làm việc trong phòng thí nghiệm phát triển các liệu pháp dựa trên tế bào từ tế bào gốc.
Sự tiến hóa của các liệu pháp tế bào và gen đang dịch chuyển mạnh mẽ từ những ý tưởng từng được xem là viễn tưởng sang thực tiễn điều trị tại các bệnh viện. Điều này đánh dấu một kỷ nguyên mới của y học hiện đại, nơi các thành phần cơ bản của cơ thể – tế bào và vật chất di truyền – được sử dụng để tăng cường hệ miễn dịch hoặc sửa chữa tận gốc nguyên nhân gây bệnh.
Trong hành trình này, một trong những thách thức lớn nhất mà ngành công nghiệp sản xuất tế bào gốc phải đối mặt là việc tạo ra các quần thể tế bào miễn dịch chuyên biệt một cách ổn định và có thể mở rộng quy mô.
Ngày 8 tháng 1 năm 2026, các nhà nghiên cứu tại Đại học British Columbia đã công bố một khám phá mang tính bước ngoặt trên tạp chí Cell Stem Cell, giải quyết rào cản kéo dài nhiều thập kỷ trong việc sản xuất tế bào T hỗ trợ (Helper T cell) từ tế bào gốc trong môi trường phòng thí nghiệm.
Vai trò “nhạc trưởng” của tế bào T hỗ trợ
Tế bào T hỗ trợ, đặc trưng bởi dấu ấn bề mặt CD4+, đóng vai trò là trung tâm điều phối của phản ứng miễn dịch thích ứng. Nhiệm vụ của chúng không phải là trực tiếp tiêu diệt vật lạ mà là phát hiện các mối đe dọa sức khỏe thông qua sự tương tác phức tạp giữa thụ thể tế bào T (TCR) và các phân tử tương hợp mô chính lớp II (MHC-II) trên các tế bào trình diện kháng nguyên. Khi được kích hoạt, tế bào T hỗ trợ giải phóng một loạt các cytokine để:
- Kích hoạt và biệt hóa tế bào B thành tương bào sản sinh kháng thể hiệu năng cao.
- Cung cấp các tín hiệu “giúp đỡ” cần thiết cho tế bào T tiêu diệt (CD8+) để tăng cường khả năng tấn công khối u.
- Thiết lập bộ nhớ miễn dịch dài hạn, giúp cơ thể ngăn chặn sự tái phát của bệnh tật.
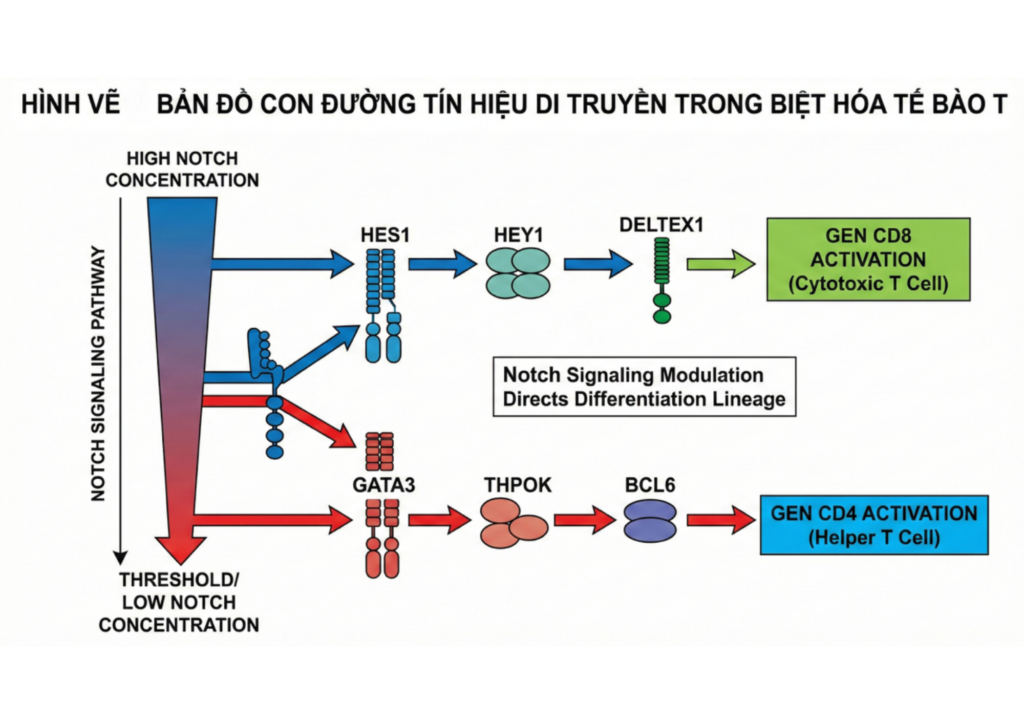
Hình: Bản đồ con đường tín hiệu di truyền trong biệt hóa tế bào T. Một sơ đồ chi tiết thể hiện các phân tử trung gian trong con đường Notch. Mũi tên xanh thể hiện sự kích hoạt gen CD8 khi Notch cao, và mũi tên đỏ thể hiện sự chuyển hướng sang gen CD4 khi nồng độ Notch được điều chỉnh giảm xuống mức ngưỡng.
Mặc dù khoa học đã đạt được những bước tiến đáng kể trong việc tạo ra tế bào T tiêu diệt từ tế bào gốc vạn năng cảm ứng (iPSCs), việc sản xuất tế bào T hỗ trợ một cách đáng tin cậy vẫn là một thách thức nan giải cho đến nay. Sự thiếu hụt loại tế bào này trong các liệu pháp tế bào hiện tại thường dẫn đến phản ứng miễn dịch không bền vững và hiệu quả điều trị thấp đối với các khối u rắn hoặc các bệnh nhiễm trùng phức tạp.
Giải mã tín hiệu Notch: Chìa khóa của sự biệt hóa
Nhóm nghiên cứu tại UBC, dẫn đầu bởi Giáo sư Peter Zandstra và Giáo sư Megan Levings, đã tập trung vào việc giải mã một trong những con đường tín hiệu cơ bản nhất của sự phát triển tế bào: con đường tín hiệu Notch. Tín hiệu Notch đóng vai trò quyết định nhưng lại có tính nhạy cảm cực cao về thời gian trong quá trình biệt hóa tế bào miễn dịch.
Qua hàng loạt các thí nghiệm sàng lọc nồng độ và thời gian thực hiện, các nhà khoa học phát hiện ra một nghịch lý sinh học: Trong khi tín hiệu Notch ở mức cao là cần thiết ở giai đoạn đầu để hướng dẫn tế bào gốc vào dòng lympho, việc duy trì tín hiệu này quá lâu sẽ “khóa” tế bào vào chương trình di truyền của dòng CD8+ và ngăn cản hoàn toàn sự hình thành của tế bào T hỗ trợ CD4+.
Bằng cách sử dụng các bộ điều biến hóa học và hệ thống nuôi cấy tự động, đội ngũ nghiên cứu đã có thể thực hiện một quy trình tinh chỉnh chính xác:
- Giai đoạn 1: Kích hoạt mạnh tín hiệu Notch để thúc đẩy tế bào gốc biệt hóa thành tiền thân tế bào T (Pro-T).
- Giai đoạn 2 (Điểm vàng): Giảm dần nồng độ tín hiệu Notch ngay tại thời điểm tế bào chuẩn bị thực hiện quyết định chọn dòng (lineage commitment).
- Giai đoạn 3: Ức chế Nocth ở mức tối thiểu để cho phép chương trình gen CD4+ được biểu hiện đầy đủ.
Đặc tính và tiềm năng của thế hệ “Thuốc sống” có sẵn
Những tế bào T hỗ trợ được nuôi cấy trong phòng thí nghiệm này không chỉ giống về mặt hình thái mà còn thể hiện các hành vi tương tự như tế bào miễn dịch thực thụ trong cơ thể người. Chúng sở hữu một kho tàng thụ thể miễn dịch (TCR) đa dạng, có khả năng nhận diện hàng triệu loại kháng nguyên khác nhau và quan trọng nhất là khả năng chuyên hóa thành các phân nhóm chức năng như Th1, Th2, hoặc Th17 tùy thuộc vào môi trường cytokine.
Thành công này mở ra cơ hội sản xuất các liệu pháp tế bào “có sẵn” (off-the-shelf) với quy mô lớn. Thay vì phải dựa vào quy trình sản xuất cá thể hóa đắt đỏ và tốn thời gian (thường mất 4-6 tuần từ lúc lấy máu bệnh nhân đến lúc có thuốc truyền), các nhà sản xuất hiện nay có thể tạo ra các ngân hàng tế bào T vạn năng từ một nguồn tế bào gốc duy nhất, sẵn sàng sử dụng ngay lập tức cho bất kỳ bệnh nhân nào.

Hình : Hệ thống phản ứng sinh học tích hợp AI cho sản xuất tế bào. Minh họa một thiết bị bioreactor hiện đại với các cảm biến quang học theo dõi mật độ tế bào và nồng độ các yếu tố tăng trưởng theo thời gian thực. Hệ thống tự động bơm các hợp chất điều hòa Notch để đảm bảo tỷ lệ biệt hóa CD4/CD8 tối ưu.
Sự kết hợp giữa tế bào T tiêu diệt và tế bào T hỗ trợ được tạo ra từ cùng một nguồn gốc tái tạo hứa hẹn sẽ tối ưu hóa hiệu quả của các liệu pháp miễn dịch thế hệ tiếp theo, đặc biệt là trong việc phá vỡ các rào cản miễn dịch của khối u rắn. Công nghệ này hiện đang trở thành nền tảng để thử nghiệm tạo ra các loại tế bào mới như tế bào T điều hòa (Tregs) cho các ứng dụng lâm sàng trong điều trị bệnh tự miễn và đào thải mảnh ghép.